谷歌DeepMind AlphaFold 3登上Nature头版,首个生物分子结构预测超越物理工具的AI系统问世...
AI科技大本营 2024-06-12 16:31:06 阅读 62

整理 | 王轶群
出品丨AI 科技大本营(ID:rgznai100)
AlphaFold 3 一经推出,就登上Nature头版,再次掀起AI学术圈巨浪。
北京时间5月8日晚间,科学顶级刊物《自然》杂志刊登了谷歌 DeepMind AlphaFold 团队和伦敦药物研发公司 Isomorphic Labs 共同署名的论文,介绍了AlphaFold 3。该平台是在AlphaFold 2模型架构以及训练系统大幅提升下,可对大量生物分子系统结构进行更准确的预测。
论文介绍了具有大幅更新的基于扩散的架构的 AlphaFold 3 模型,该模型能够对包括蛋白质、核酸、小分子、离子和修饰残基在内的复合物进行联合结构预测。新的 AlphaFold 模型比许多以前的专用工具显著提高了准确性:蛋白质-配体相互作用的准确性比最先进的对接工具高得多,蛋白质-核酸相互作用的准确性比核酸特异性预测器高得多,并且在抗体-抗原预测准确性上明显高于 AlphaFold-Multimer v2.3。这些结果共同表明,在单个统一的深度学习框架内可以实现跨生物分子空间的高精度建模。

论文地址:https://www.nature.com/articles/s41586-024-07487-w
谷歌DeepMind联合创始人、CEO Demis Hassabis表示:“AlphaFold 3的发布是一个重要的里程碑,在AI理解和建模生物学的道路上,AI又迈出了重要一步!”

超越蛋白质折叠的革命性系统
AlphaFold 3 无疑是一款革命性的系统。
AlphaFold首次于2020年问世,AlphaFold是单链蛋白质预测的根本性突破。之后AlphaFold-Multimer扩展到具有多个蛋白质链的复合物,再后是 AlphaFold2.3,它提高了性能并将覆盖范围扩大到更大的复合物。
不过,扩大单一深度学习模型能预测的复合物一直很难,因为不同类型的特异性相互作用差异太大。此次发布的AlphaFold 3,能预测蛋白质与其他蛋白质、核酸、小分子、离子、修饰蛋白质残基的复合物,以及抗体-抗原的相互作用。
同时,AlphaFold 3全新的蛋白质结构预测系统能以前所未有的精度预测“蛋白质数据库(Protein Data Bank)”内几乎所有分子类型的复合物结构。
也就是说,所有生物分子结构都可以预测。
更重要的是,对于蛋白质与其他分子类型的相互作用,AlphaFold 3在基准测试中的准确率比现有最好的传统方法高出50%,且无需输入任何结构信息。对一些重要的相互作用类型,AlphaFold 3的预测精度甚至可以提升100%。
至此,AlphaFold 3成为首个在生物分子结构预测方面超越基于物理工具的方法的人工智能系统。
7R6R - DNA 结合蛋白:AlphaFold 3 对分子复合物的预测,其特征是蛋白质(蓝色)与 DNA 双螺旋(粉色)结合,与通过艰苦实验发现的真实分子结构(灰色)近乎完美匹配。
这次AlphaFold 3使用的,还是AI革命最核心的组合架构Transformer+Diffusion。为了创建 AlphaFold3、Jumper,DeepMind 首席执行官 Demis Hassabis 及其同事对其前身进行了重大更改:例如,最新版本更少依赖于与目标序列相关的蛋白质信息。AlphaFold3 还使用一种称为扩散模型的机器学习网络,由 Midjourney 等图像生成人工智能使用。“这是一个相当大的变化,”Jumper 说。
研究人员发现,AlphaFold3 在预测蛋白质及其伙伴的结构方面远远优于现有的软件工具。例如,科学家——尤其是那些对寻找新药感兴趣的科学家——通常使用“对接”软件来物理模拟化学物质与蛋白质的结合程度(通常借助蛋白质实验确定的结构)。AlphaFold3 被证明优于两个对接程序,以及另一个名为 RoseTTAFold All-Atom 的基于人工智能的工具。
Uhlmann 的团队使用 AlphaFold3 来预测参与复制基因组的 DNA 相互作用蛋白的结构,这是细胞分裂所必需的步骤。乌尔曼说,通过蛋白质突变来改变这种相互作用的实验表明,这些预测通常是正确的。“这是一个令人惊奇的发现工具,”他补充道。
“AlphaFold 3 的结构预测性能非常令人印象深刻,”西雅图华盛顿大学的计算生物物理学家 David Baker 说道。他补充道,它比他的团队开发的 RoseTTAFold All-Atom 更好。
8AW3 - RNA 修饰蛋白:AlphaFold 3 对具有蛋白质(蓝色)、RNA 链(紫色)和两个离子(黄色)的分子复合物的预测与真实结构(灰色)非常匹配。这种复合物涉及其他蛋白质的产生——这是生命和健康的基础细胞过程。

加速实现下一个“数字生物学”时代
下图展示了 AlphaFold 的卓越能力,可以预测蛋白质折叠之外的精确结构,生成跨配体、蛋白质、核酸和翻译后修饰的高度准确的结构预测。
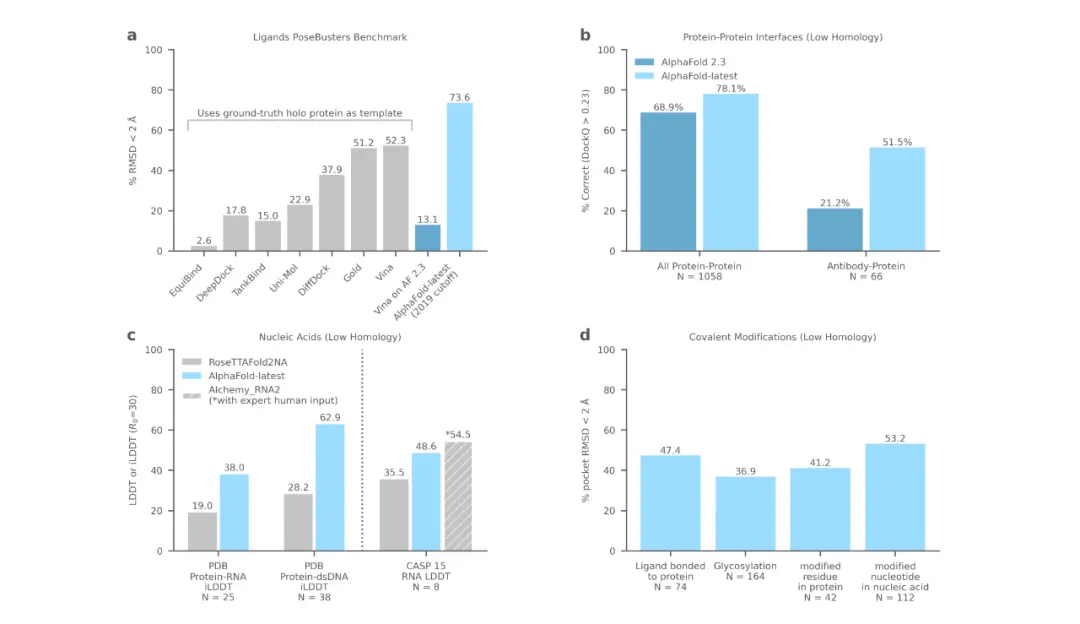
蛋白质-配体复合物 (a)、蛋白质 (b)、核酸 (c) 和共价修饰 (d) 的性能。
AlphaFold 3还可以模拟细胞之间化学变化,以控制细胞的正常运转,预防疾病发生。
该模型扩展的功能和性能有助于加速生物医学突破并实现下一个“数字生物学”时代——为疾病途径、基因组学、生物可再生材料、植物免疫、潜在治疗靶点、药物设计机制和机制的功能提供新的见解。用于实现蛋白质工程和合成生物学的新平台。
7PNM - 普通感冒病毒(冠状病毒 OC43)的刺突蛋白:AlphaFold 3 对感冒病毒刺突蛋白(蓝色)与抗体(绿松石色)和单糖(黄色)相互作用时的结构预测,与真实结构准确匹配(灰色的)。动画显示蛋白质与抗体相互作用,然后与糖相互作用。增进我们对此类免疫系统过程的了解有助于更好地了解包括 COVID-19 在内的冠状病毒,从而提高改进治疗的可能性。
AlphaFold 3已在Isomorphic Labs,实现了高度准确预测配体-受体相互作用,并帮助他们构想药物发现的过程。
Isomorphic Labs 是一家位于伦敦的 DeepMind 衍生公司,它正在使用 AlphaFold3 通过自己的管道或与其他制药公司合作开发药物。Isomorphic Labs 官网表示,该公司正在将下一代 AlphaFold 模型应用于治疗药物设计,帮助快速准确地表征对治疗疾病很重要的多种类型的大分子结构。
7BBV - 酶:AlphaFold 3 对分子复合物的预测,包括酶蛋白(蓝色)、离子(黄色球体)和单糖(黄色)以及真实结构(灰色)。这种酶存在于一种土传真菌(大丽轮枝菌)中,它会损害多种植物。深入了解这种酶如何与植物细胞相互作用可以帮助研究人员开发更健康、更有弹性的作物。

开放与商业化的平衡:
“生物学研究的AI突破价值千亿美元”
谷歌DeepMind还推出了免费研究平台“AlphaFold Server”,供全球科学家非商业化研究。
不论每个人的技术专长如何,只需点击几下,就可以利用AlphaFold 3在10分钟内预测分子,并测试假设。
伦敦弗朗西斯·克里克研究所的生物化学家弗兰克·乌尔曼(Frank Uhlmann)很早就接触到了 AlphaFold3,他对其功能印象深刻。“这简直是革命性的,”他说。“这将使结构生物学研究民主化。”
与RoseTTAFold和AlphaFold2不同,科学家将无法运行他们自己版本的AlphaFold3,AlphaFold3底层的代码或训练模型后获得的其他信息也不会被公开。相反,研究人员将可以访问“AlphaFold3服务器”,他们可以在其中输入他们选择的蛋白质序列以及一系列辅助分子。
Uhlmann 很喜欢他迄今为止所看到的服务器,他说这比他在他的研究所访问的 AlphaFold2 版本更简单、更快。“你上传它,10 分钟后,你就得到了结构,”他说。对于大多数科学家来说,“服务器真的会毁掉它。每个人都可以做到。”
然而,对 AlphaFold3 服务器的访问是有限的。目前科学家每天只能进行 10 次预测,而且不可能获得与可能的药物结合的蛋白质结构。
DeepMind 的人工智能科学主管兼研究合作伙伴 Pushmeet Kohli 表示:“我们必须在确保其可获取性并在科学界产生影响以及不损害 Isomorphic 追求商业药物发现的能力之间取得平衡。”
2022 年,AlphaFold 与 EMBL 的欧洲生物信息学研究所 (EMBL-EBI) 合作,通过AlphaFold 蛋白质结构数据库免费提供对科学已知的几乎所有编目蛋白质的结构预测。
截至目前,全球已经有180+万的科学家使用 AlphaFold 加速研究,包括开发生物可再生材料,或推进基因研究。此前,截止2023年10月底,已有 190 多个国家的 140 万用户访问了 AlphaFold 数据库,世界各地的科学家已利用 AlphaFold 的预测来帮助推进各个方面的研究,从加速新型疟疾疫苗和推进癌症药物的发现,到开发用于解决污染的食塑料酶。
值得注意的是,AlphaFold也是谷歌 DeepMind 重要的商业化目标业务之一,DeepMind 首席执行官正通过 AlphaFold 瞄准 1000 亿美元以上的人工智能药物发现业务。
“我希望通过 Isomorphic 实现这两件事:建立一个价值数千亿美元的业务——我认为它有这个潜力——并且为社会和人类带来难以置信的好处。”Demis Hassabis 表示,生物学研究领域的人工智能突破可能是一项价值数千亿美元的业务,将通过 DeepMind 衍生公司 Isomorphic Labs 实现商业化。Demis Hassabis 表示,首批人工智能设计的药物可能会在“未来几年”内准备好进行测试。他表示,人工智能系统有可能彻底改变医学,并创造“巨大的商业价值”。
谷歌发布博客表示:“AlphaFold 3 和我们的免费 AlphaFold 服务器的影响将通过它们如何帮助科学家加速发现生物学中的未决问题和新的研究领域来实现。我们刚刚开始挖掘 AlphaFold 3 的潜力,迫不及待地想看看未来会怎样。”
参考链接:
https://www.nature.com/articles/d41586-024-01383-z
https://www.isomorphiclabs.com/articles/a-glimpse-of-the-next-generation-of-alphafold
https://blog.google/technology/ai/google-deepmind-isomorphic-alphafold-3-ai-model/#life-molecules


上一篇: 我常用的几款免费AI生成视频平台
本文标签
声明
本文内容仅代表作者观点,或转载于其他网站,本站不以此文作为商业用途
如有涉及侵权,请联系本站进行删除
转载本站原创文章,请注明来源及作者。